Định luật bảo toàn khối lượng là gì
“ Trong một phản ứng hóa học, tổng khối lượng của các sản phẩm bằng tổng khối lượng của các chất phản ứng”
Giả sử có phản ứng giữa A + B tạo ra C + D có công thức khối lượng được viết như sau :
VD: Bari clorua +natri sunphat bari sunphat + natri clorua. Có CT khối lượng là:
mbari clorua + mnatri sunphat = mbari sunphat + mnatri clorua
2. Áp dụng: trong một phản ứng có n chất, nếu biết khối lượng của (n – 1) chất thì tính được khối lượng của chất còn lại.
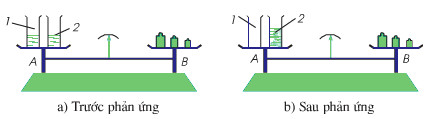 Phản ứng hóa học trong cốc trên đĩa cân
Phản ứng hóa học trong cốc trên đĩa cân
• Thực hiện thí nghiệm như sau:
– Đặt 2 cốc chứa dd BaCl2 và Na2SO4 lên 1 đĩa cân
– Đặt các quả cân lên đĩa cân còn lại.
– Đổ cốc đựng dung dịch BaCl2 vào cốc đựng dung dịch Na2SO4
• Quan sát thấy, có chất màu trắng xuất hiện, đó là bari sunfat BaSO4, chất này không tan, đã xảy ra phản ứng hóa học sau:
Bari clorua + Natri sunfat → Bari sunfat + Natri clorua
• Kim cân ở vị trí thăng bằng.
Cách tính định luật bảo toàn khối lượng
– Giả sử có phương trình phản ứng: A + B → C + D
– Công thức tính của định luật bảo toàn khối lượng như sau:
Trong đó: mA; mB; mC; mD là khối lượng của mỗi chất.
Thí dụ, công thức về khối lượng của các chất phản ứng trong thí nghiệm là:
mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
– Trong công thức này, nếu biết khối lượng của 3 chất thì ta tính được khối lượng của chất còn lại. Gọi a, b, c lần lượt là khối lượng của Bari Clorua, Natri Sunfat và Natri Clorua. Và x là số mol của Bari Sunfat.
Ta có: a + b = c + x suy ra x = a + b – c;…
Bài tập về định luật bảo toàn khối lượng
Bài 1 trang 54 SGK Hóa học 8: a) Phát biểu định luật bảo toàn khối lượng.
b) Giải thích vì sao khi một phản ứng hóa học xảy ra khối lượng được bảo toàn.
° Lời giải bài 1 trang 54 SGK Hóa học 8:
a) Phát biểu định luật bảo toàn khối lượng: “Trong một phản ứng hóa học, tổng khối lượng của các sản phẩm bằng tổng khối lượng các chất phản ứng”.
b) Một phản ứng hóa học xảy ra khối lượng được bảo toàn vì trong phản ứng hóa học nguyên tử được bảo toàn.
Bài 2 trang 54 SGK Hóa học 8: Trong phản ứng ở thí nghiệm trên, cho biết khối lượng của natri sunfat Na2SO4 là 14,2g khối lượng của các sản phẩm bari sunfat BaSO4 và natri clorua NaCl theo thứ tự là 23,3g và 11,7g. Hãy tính khối lượng của Bari clorua BaCl2 đã phản ứng.
° Lời giải bài 2 trang 54 SGK Hóa học 8:
– Phương trình phản ứng của thí nghiệm:
Natri sunfat + Bari clorua → Bari sunfat + Natri clorua
– Theo định luật bảo toàn khối lượng, ta có:
mBaCl2 + mNa2SO4 = mBaSO4 + mNaCl
⇒ mBaCl2 = mBaSO4 + mNaCl – mNa2SO4 = 23,3 + 11,7 – 14,2 = 20,8g.
* Bài 3 trang 54 SGK Hóa học 8: Đốt cháy hết 9g kim loại magie Mg trong không khí thu được 15g hợp chất magie oxit MgO. Biết rằng magie cháy là phản ứng với khí oxi O2 trong không khí.
a) Viết công thức về khối lượng của phản ứng xảy ra.
b) Tính khối lượng của khí oxi đã phản ứng.
° Lời giải bài 3 trang 54 SGK Hóa học 8:
– Đề cho: mMg = 9(g); mMgO = 15(g)
a) Theo định luật bảo toàn khối lượng: mMg + mO2 = mMgO.
b) Từ định luật bảo toàn khối lượng ta suy ra: mO2= mMgO – mMg = 15 – 9 = 6(g).